Es ist eines der wichtigsten Enzyme in der medizinischen Diagnostik: Die sogenannte „Horseradish Peroxidase“ (Meerrettichperoxidase) wird für viele Medizinprodukte verwendet – oft kommt sie zum Einsatz, wenn ein Farbwechsel eines Teststreifens das Vorhandensein von Antikörpern oder anderen Proteinen nachweisen soll.
Gerade in letzter Zeit herrscht aber immer wieder Mangel an Horseradish Peroxidase. Sie wird nämlich derzeit aus Krenwurzeln gewonnen, und das hat große Nachteile: Der landwirtschaftliche Ertrag ist nicht immer gleich, die Wurzeln produzieren nicht bloß eine Version des Enzyms, sondern eine ganze Familie ähnlicher Enzyme, und das in variierender Menge. Daher versuchte man an der TU Wien, eine verlässliche, präzise Synthesemethode im Labor zu entwickeln. Nach jahrelanger Forschungsarbeit ist das nun gelungen: Die Herstellung von Horseradish Peroxidase ist nun mit Hilfe von E. coli-Bakterien möglich. Dabei entsteht auf exakt reproduzierbare Weise ausschließlich ein ganz bestimmtes Enzym, das Verfahren lässt sich auf großindustriellen Maßstab skalieren. Zwei Patente dafür sind bereits angemeldet, nun sucht die TU Wien nach Industriepartnern.
Unberechenbares Gemüse
„Wenn man Horseradish Peroxidase aus Pflanzen gewinnt, erhält man keine chemisch exakt definierte Substanz“, sagt Prof. Oliver Spadiut vom Institut für Verfahrenstechnik, Umwelttechnik und technische Biowissenschaften der TU Wien. „Je nach Umweltbedingungen erzeugt die Pflanze unterschiedliche Mengen unterschiedlicher Enzyme.“ Für bestimmte medizinische Einsatzgebiete lassen sich solche Substanzen gar nicht verwenden, man darf ein solches undefiniertes Gemisch verschiedener Enzyme beispielsweise nicht einem Menschen injizieren.
In der medizinischen Diagnostik sind die Regeln weniger streng, und so wird Horseradish Peroxidase etwa für Western Blots oder das ELISA-Verfahren verwendet – bei diesen Techniken werden zum Beispiel bestimmte Antikörper an das Enzym angekoppelt. Der Antikörper dockt an einem gesuchten Molekül an, das Enzym sorgt dann für einen Farbumschlag. So kann das Vorhandensein bestimmter Moleküle farblich sichtbar gemacht werden.
„Wir erleben derzeit weltweit Engpässe bei der Versorgung mit diesem Enzym“, sagt Oliver Spadiut. „Das hat auch mit dem Klimawandel und schlechten Ernten zu tun, bei anderen Umweltbedingungen ändert die Pflanze auch die Zusammensetzung der erzeugten Enzyme auf schwer vorhersagbare Weise.“ Gleichzeitig steigt aber die globale Nachfrage: Auf über 90 Millionen Euro pro Jahr wird das Marktvolumen geschätzt, das der Handel mit Horseradish Peroxidase in den nächsten Jahren erreichen wird.
Ein Bakterium als Rettung
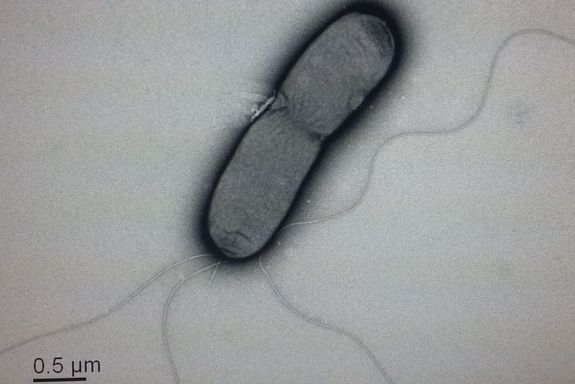
Oliver Spadiut machte sich daher schon vor Jahren mit seinem Team an die Arbeit, um ein synthetisches Herstellungsverfahren für das wertvolle Enzym zu entwickeln. Das Gen für die Herstellung von Horseradish Peroxidase wurde im Labor in Hefezellen, Säugetierzellen und E. coli-Zellen eingebaut. Alle drei Varianten lieferten tatsächlich das gewünschte Enzym, als technisch beste Lösung erwies sich die Verwendung von E. coli – einem bestens bekannten Bakterium, das in der Biotechnologie auch bisher schon oft mit großem Erfolg eingesetzt wurde.
Allerdings entsteht dabei zunächst noch kein funktionsfähiges Enzym, sondern ein sogenanntes „Einschlusskörperchen“ – ein Protein, das biochemisch zwar dem gewünschten Enzym entspricht, aber nicht korrekt gefaltet ist. Man muss also in einem weiteren Schritt das Einschlusskörperchen entwirren und dann in die richtige Form bringen, ähnlich als würde man einen Wollknäuel zunächst auswickeln und dann zu einem wohlgeordneten Wolle-Ball zusammenrollen.
Besonders auf diesem Forschungsgebiet, der Verarbeitung von Einschlusskörperchen, verfügt Oliver Spadiuts Team über viel Erfahrung – und so gelang es an der TU Wien weltweit zum ersten Mal, ein zuverlässiges, reproduzierbares Verfahren für die Herstellung von Horseradish Peroxidase zu entwickeln. Die Patente sind bereits angemeldet, das Verfahren ist technisch ausgereift. „Wir könnten morgen damit beginnen, die Methode auf industrieller Skala anzuwenden“, sagt Oliver Spadiut. „Wir haben hier nicht bloß ein theoretisches Konzept, sondern eine erprobte Methode, die reif für die industrielle Anwendung ist.“
Nächster Schritt: Krebstherapie?
Nachdem es nun gelingt, Horseradish Peroxidase auf genau definierte, hochreine Weise zu produzieren, sind damit nun auch ganz andere Anwendungen jenseits der Diagnostik denkbar. „Man könnte zum Beispiel die Horseradish Peroxidase nun auch für die Krebstherapie einsetzen, indem man sie an Antikörper koppelt, die dann ganz spezifisch an Krebszellen andocken“, sagt Oliver Spadiut. „Wir gehen daher davon aus, dass das Marktvolumen von Horseradish Peroxidase durch viele neue Anwendungen sogar noch drastisch steigen könnte.“ Spadiut möchte nun mit interessierten Pharmaunternehmen Gespräche führen, um die technologische Anwendung der neuen Erfindung möglichst rasch in die Wege zu leiten.
Die Patentierung erfolgt mit Unterstützung des Forschungs- und Transfersupports der TU Wien.